除致命脑瘤!《科学》:创新CAR-T有望变革治疗格局
日前,《科学》杂志同时刊载了两项有关CAR - T细胞的重要研究成果。科学家们运用合成生物学策略,极大地拓宽了利用免疫细胞治疗疾病的可能性范围。经过改造后的CAR - T细胞具备强大的功能,它们不仅能够突破屏障进入大脑,从而消除致命的脑瘤,而且还可用于多发性硬化症的治疗,甚至有助于改善器官移植以及各类自身免疫疾病的治疗效果。
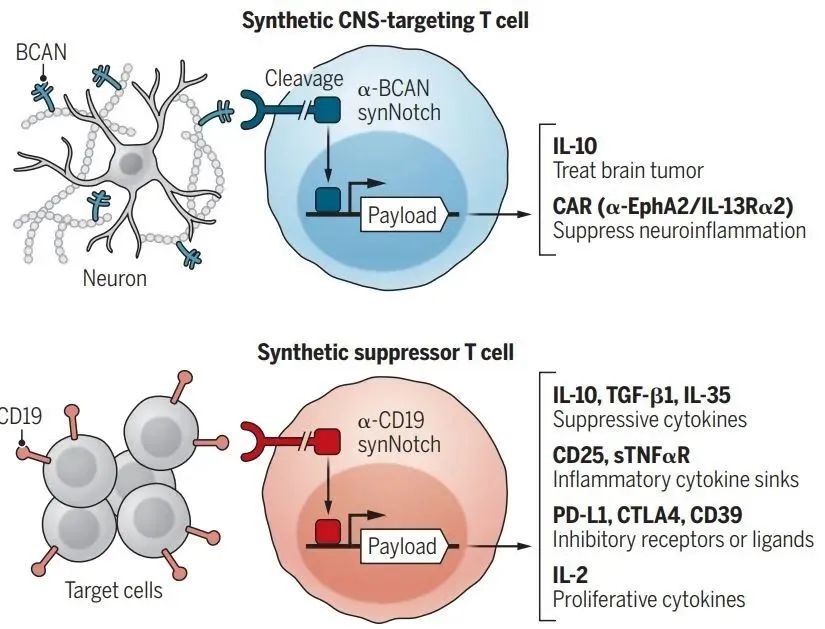
▲基于合成生物学策略设计的两种工程化T细胞(图片来源:参考资料[2])
CAR - T是近年来备受瞩目的明星抗癌疗法。这种疗法的实施,首先要从患者体内分离出免疫T细胞,然后在体外对这些T细胞进行基因改造,为其装配上能够识别癌细胞表面抗原的“嵌合抗原受体”(CAR)。接着,经过改造的细胞会在实验室里大量增殖,最后再被输回患者体内,犹如精准的导弹一般,瞄准癌细胞发起猛烈的攻击。
自2017年美国食品药品监督管理局(FDA)批准首款CAR - T疗法上市以来,现有的多款CAR - T疗法已经使白血病、淋巴瘤和多发性骨髓瘤等血液癌症患者受益。
不过,研究人员也清楚,CAR - T疗法并非包治百病的万能药。传统的CAR - T细胞存在靶点过于特异这一局限性,这对CAR - T细胞发挥作用造成了很大的阻碍。因为CAR必须靶向肿瘤细胞表面特有的抗原,这样才能精确地识别并清除肿瘤细胞。但很多时候,非肿瘤组织也可能会表达相同的抗原蛋白,如此一来,就有可能对健康组织造成误伤。
在首篇论文里,加州大学旧金山分校(UCSF)的研究团队为杀伤性T细胞打造出一种可编程的导航定位体系。借助该体系,这些免疫细胞能够直接抵达大脑以杀伤肿瘤细胞,并且不会对其他健康组织产生毒性。

据研究人员介绍,他们凭借基因电路设计出的这套导航定位系统,具备同时识别大脑的“邮政编码”和肿瘤的“街道地址”的能力。
装配了导航功能的T细胞,一开始会搜索一种名为brevican(BCAN)的蛋白质。这种蛋白质仅存在于大脑之中,是大脑特有的细胞外基质的组成部分,就如同大脑专属的邮政编码。接着,这些免疫细胞会检测脑瘤特有的一种蛋白,例如胶质瘤相关抗原EphA2。只有精准定位到肿瘤之后,它们才会开启表达CAR的基因,从而消除不断增殖的肿瘤。
与之相反,当这些CAR - T细胞还处于血液中时,由于“邮政编码”不匹配,即便其他正常组织的细胞恰好也有相同的蛋白“地址”,这些CAR - T细胞仍然会处于休眠状态,进而避免了外周或全身毒性。
利用这些靶向脑部的CAR - T细胞,研究人员率先对胶质母细胞瘤的治疗可能性进行了测试。胶质母细胞瘤是一种极其难治的脑瘤,血脑屏障的存在致使药物难以进入大脑内部发挥功效,众多常规疗法也难以达到理想的治疗效果。在此次研究中,小鼠实验表明,经过改造的CAR - T细胞能够顺利进入小鼠大脑,清除原发性胶质母细胞瘤。
更为重要的是,在肿瘤消退后的数周到数月期间,这些CAR - T细胞依然存活,展现出持久的抗肿瘤反应。研究人员将新的肿瘤细胞植入小鼠大脑后,发现CAR - T细胞仍然能够发现并杀灭新的肿瘤。这表明它具有预防癌症复发的潜力,也意味着同样的策略可用于清除转移到脑部的肿瘤,例如乳腺癌的脑转移病灶。
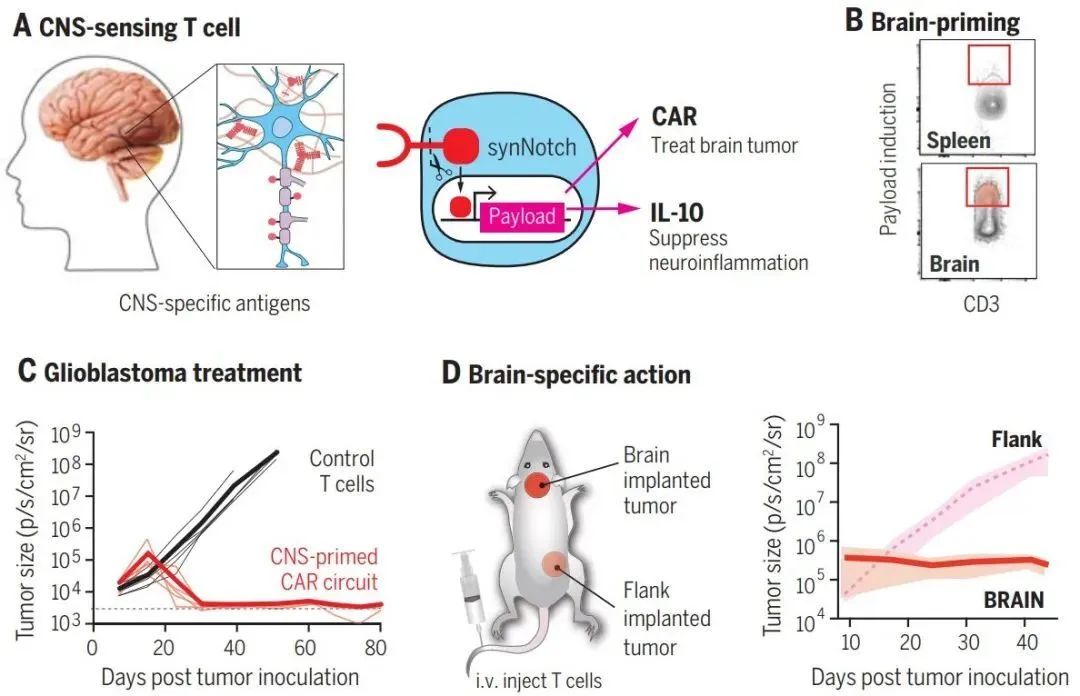
▲研究示意图(图片来源:参考资料[1])
除了治疗癌症,这套可编程的大脑靶向系统还有另一种用途:让T细胞改为输送抗炎分子,从而治疗多发性硬化。多发性硬化是一种自身免疫疾病,免疫系统异常攻击脑、脊髓等中枢神经系统的神经细胞的髓鞘,导致炎症和损伤。在多发性硬化小鼠模型中,靶向BCAN的T细胞进入大脑后释放具有免疫抑制作用的细胞因子IL-10,可以改善小鼠的神经炎症。
另一篇论文中,另一支加州大学旧金山分校的科研团队旨在让免疫系统保持平衡,他们将CAR设计应用于调节性T细胞,使其精确调控免疫反应,还能清除炎症分子。

为此,研究人员首先给CD4 T细胞装上识别胰岛细胞的“导航”分子,然后使其产生抑制性的分子,例如TGFβ和CD25,以此阻止杀伤性T细胞对胰岛细胞的攻击。这种设想在论文中获得了概念验证,作者模拟1型糖尿病的治疗方法,将人类胰岛细胞移植到小鼠体内,然后输入改造后的CD4 T细胞。结果显示,这些CAR-T细胞在体内成功找到了人类胰岛细胞,并帮助它们避开免疫排斥,存活下来。
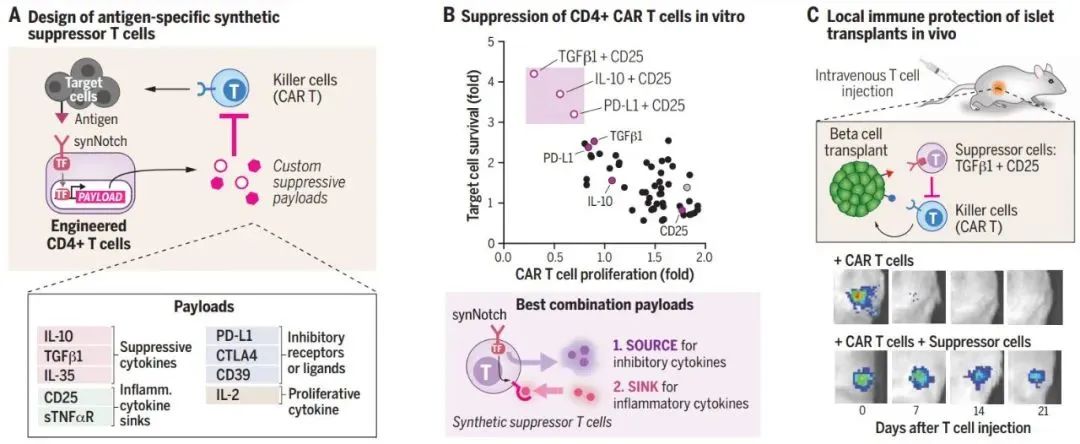
▲研究示意图(图片来源:参考资料[2])
除了用于1型糖尿病和其他自身免疫疾病外,这项技术同样可以应用于癌症治疗,让CAR-T细胞只攻击肿瘤,不攻击健康组织。
正如《自然》同期评论文章所总结的,这项概念验证研究为免疫抑制T细胞治疗自身免疫疾病、器官排斥和CAR-T细胞毒性提供了前景广阔的新途径。
【参考资料】
[1] Milos S. Simic et al., Programming tissue-sensing T cells that deliver therapies to the brain. Science (2024) Doi: 10.1126/science.adl4237
[2] Nishith R. Reddy et al., Engineering synthetic suppressor T cells that execute locally targeted immunoprotective programs. Science (2024) Doi: 10.1126/science.adl4793
[3] Synthetic gene circuits drive disease-fighting T cells. Science (2024) Doi: 10.1126/science.adt9921